இரசாயன சேர்மங்களுக்கு பெயரிடுவது எப்படி
நூலாசிரியர்:
Laura McKinney
உருவாக்கிய தேதி:
2 ஏப்ரல் 2021
புதுப்பிப்பு தேதி:
26 ஜூன் 2024

உள்ளடக்கம்
- நிலைகளில்
- முறை 1 அயனி சேர்மங்களின் பெயரிடல்
- முறை 2 பாலிடோமிக் சேர்மங்களின் பெயரிடல்
- முறை 3 கோவலன்ட் சேர்மங்களின் பெயரிடல்
வேதியியல் துறையில் வெற்றி பெறுவதற்கு அடிப்படை வேதியியல் சேர்மங்களை எவ்வாறு பெயரிடுவது என்று தெரிந்து கொள்ள வேண்டும். இந்த வழிகாட்டி வேதியியல் சேர்மங்களுக்கான பெயரிடும் செயல்முறை மற்றும் உங்களுக்கு அறிமுகமில்லாத சேர்மங்களுக்கு பெயர்களை எவ்வாறு ஒதுக்குவது என்பது குறித்த அடிப்படை விதிகளை உங்களுக்கு வழங்குகிறது.
நிலைகளில்
முறை 1 அயனி சேர்மங்களின் பெயரிடல்
- அயனி கலவை என்றால் என்ன? அயனி கலவைகள் ஒரு உலோகம் மற்றும் ஒரு உலோகம் அல்லாதவை. கலவையில் உள்ள உறுப்புகளுக்கு எந்த வகைகள் உள்ளன என்பதை அறிய கால உறுப்புகளின் கால அட்டவணையைப் பார்க்கவும்.
-

பெயரை உருவாக்குங்கள். இரண்டு உறுப்புகளின் அயனி கலவைக்கு பெயரிடுவதை விட எதுவும் எளிதானது அல்ல. உண்மையில், சேர்மத்தின் பெயரின் முதல் பகுதி "யூரே" என்ற பின்னொட்டைத் தாங்கிய உலோகமற்ற தனிமத்தின் பெயருடன் ஒத்திருக்கிறது, இரண்டாவது உலோக உறுப்பு பெயருடன் ஒத்திருக்கிறது. விதிவிலக்குகள் உள்ளன: ஆக்சைடு, பாஸ்பைடு, நைட்ரைடு, சல்பைடு.- எடுத்துக்காட்டு: அல்2ஓ3. அல்2 = அலுமினியம்; ஓ3 = ஆக்ஸிஜன். எனவே கலவையின் பெயர் "அலுமினியம் ஆக்சைடு".
-
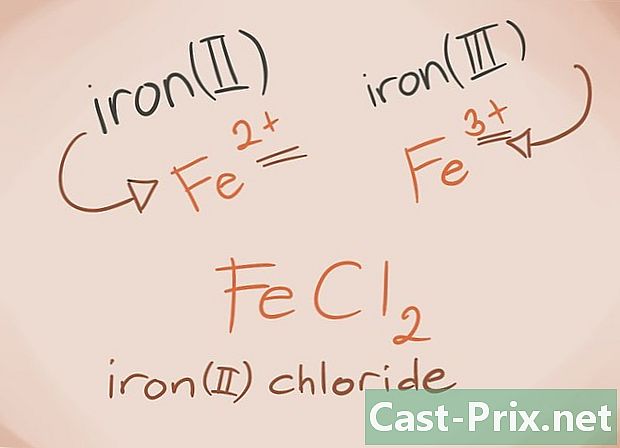
இடைநிலை உலோகங்களை அறிந்து கொள்ளுங்கள். இடைக்கால உலோகங்கள் கால அட்டவணையின் டி மற்றும் எஃப் தொகுதிகளில் காணப்படுகின்றன. கலவை என்ற பெயரில், இந்த உலோகங்களின் கட்டணம் ரோமானிய எண்களில் எழுதப்பட்டுள்ளது. ஏனென்றால், மாற்றம் உலோகங்கள் அதிக சுமையைச் சுமந்து, மேலும் ஒரு சேர்மத்தை உருவாக்க முடியும்.- எடுத்துக்காட்டு: FeCl2 மற்றும் FeCl3. Fe = இரும்பு; cl2 = -2 குளோரைடு; cl3 = குளோரைடு -3. பெயர்களாக, ஃபெரஸ் குளோரைடு (II) மற்றும் ஃபெரிக் குளோரைடு (III) இருக்கும்.
முறை 2 பாலிடோமிக் சேர்மங்களின் பெயரிடல்
-

பாலிடோமிக் கலவை என்றால் என்ன என்பதை நீங்கள் புரிந்து கொள்ள வேண்டும். பாலிடோமிக் சேர்மங்கள் ஒருவருக்கொருவர் தொடர்புடைய டேட்டோம்களின் குழுவால் உருவாக்கப்பட்ட கலவைகள்; கட்டணம் வசூலிக்கும் முழுக் குழுவும் நேர்மறை அல்லது எதிர்மறை. பாலிடோமிக் சேர்மங்களில் நீங்கள் செலுத்தக்கூடிய மூன்று அடிப்படை செயல்கள் உள்ளன:- கலவையின் முதல் பகுதிக்கு நீங்கள் ஒரு ஹைட்ரஜனை சேர்க்கலாம். "ஹைட்ரஜன்" என்ற சொல் உண்மையில் கலவையின் பெயரின் தொடக்கத்தில் சேர்க்கப்பட்டுள்ளது. இது எதிர்மறை கட்டணத்தின் மதிப்பை ஒவ்வொன்றாகக் குறைக்கும். எடுத்துக்காட்டாக, "கார்பனேட்" CO3 "ஹைட்ரஜன் கார்பனேட்" HCO ஆக மாறுகிறது3.

- நீங்கள் கலவையிலிருந்து ஆக்ஸிஜனையும் அகற்றலாம். சுமை மாற்றப்படவில்லை, ஆனால் கலவையின் "-ate" பின்னொட்டு "-ique" ஆக மாற்றப்பட்டுள்ளது. எடுத்துக்காட்டாக இதன் மாற்றம்: இல்லை3 இல்லை2 நாம் நைட்ரேட்டிலிருந்து நைட்ரேட்டுக்கு செல்கிறோம். "

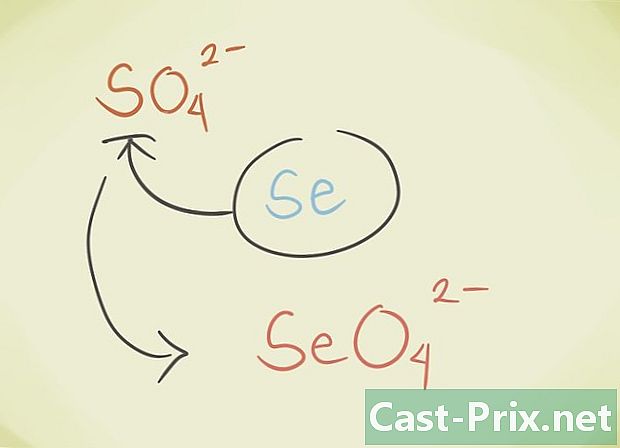
- கலவையின் மைய லேட்டோமை அதே காலக் குழுவிற்கு சொந்தமான மற்றொரு அணுவுடன் மாற்றலாம். உதாரணமாக, SO சல்பேட்4 செலினேட் எஸ்சிஓ மூலம் மாற்றலாம்4.
- கலவையின் முதல் பகுதிக்கு நீங்கள் ஒரு ஹைட்ரஜனை சேர்க்கலாம். "ஹைட்ரஜன்" என்ற சொல் உண்மையில் கலவையின் பெயரின் தொடக்கத்தில் சேர்க்கப்பட்டுள்ளது. இது எதிர்மறை கட்டணத்தின் மதிப்பை ஒவ்வொன்றாகக் குறைக்கும். எடுத்துக்காட்டாக, "கார்பனேட்" CO3 "ஹைட்ரஜன் கார்பனேட்" HCO ஆக மாறுகிறது3.
-

மிகவும் பொதுவான டியான் குழுக்களை நினைவில் கொள்ளுங்கள். கீழேயுள்ள குழுக்கள் பெரும்பாலான பாலிடோமிக் சேர்மங்களை உருவாக்கப் பயன்படுத்தப்படுகின்றன. அவற்றின் எதிர்மறை கட்டணத்தின் அதிகரிக்கும் வரிசையைப் பின்பற்றி, எங்களிடம்:- ஹைட்ராக்சைடு அயனிகள்: OH
- நைட்ரேட் அயனிகள்: இல்லை3
- ஹைட்ரஜன் கார்பனேட் அயனிகள்: HCO3
- பெர்மாங்கனேட் அயனிகள்: MnO4
- கார்பனேட் அயனிகள்: CO3
- குரோமேட் அயனிகள்: CrO4
- டைக்ரோமேட் அயனிகள்: சி.ஆர்2ஓ7
- சல்பேட் அயனிகள்: SO4
- சல்பைட் அயனிகள்: SO3
- தியோசல்பேட் அயனிகள்: எஸ் 2 ஓ3
- பாஸ்பேட் அயனிகள்: பி.ஓ.4
- அம்மோனியம் அயனிகள்: என்.எச்4
- மேலே உள்ள பட்டியலிலிருந்து கூட்டு பெயர்களை உருவாக்குங்கள். குழு தொடர்பான எந்தவொரு பொருட்களுடனும் ஒரு பெயர் சங்கத்தை உருவாக்குங்கள். உறுப்பு அயனிக் குழுவின் முன் வைக்கப்பட்டால், உறுப்பு பெயர் வெறுமனே கூட்டு பெயரின் தொடக்கத்தில் சேர்க்கப்படும்.
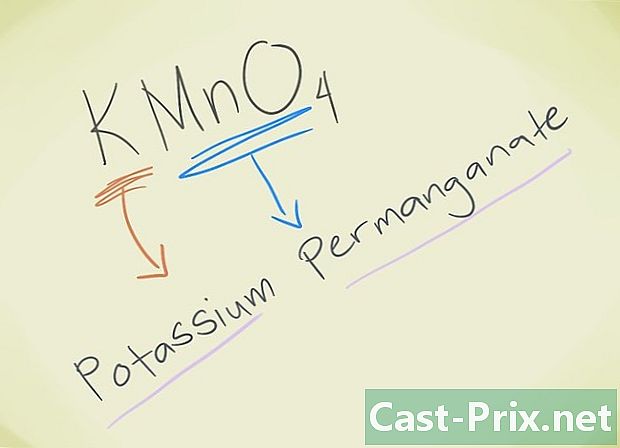
- எடுத்துக்காட்டு: KMnO4. அந்த சிங்கம் MnO ஐ நீங்கள் அறிந்து கொள்ள வேண்டும்4 சிங்கம் பெர்மாங்கனேட்டுக்கு ஒத்திருக்கிறது. கே என்பது பொட்டாசியத்தை குறிக்கிறது. எனவே உங்கள் கலவை பெர்மங்கனேட் பொட்டாசியம் என்று அழைக்கப்படும்.
- எடுத்துக்காட்டு: NaOH. இது ஓஹோ என்று நீங்கள் இங்கே புரிந்துகொண்டிருப்பீர்கள். Na என்பது சோடியம், எனவே கலவை சோடியம் ஹைட்ராக்சைடு என்று அழைக்கப்படும்.

- எடுத்துக்காட்டு: KMnO4. அந்த சிங்கம் MnO ஐ நீங்கள் அறிந்து கொள்ள வேண்டும்4 சிங்கம் பெர்மாங்கனேட்டுக்கு ஒத்திருக்கிறது. கே என்பது பொட்டாசியத்தை குறிக்கிறது. எனவே உங்கள் கலவை பெர்மங்கனேட் பொட்டாசியம் என்று அழைக்கப்படும்.
முறை 3 கோவலன்ட் சேர்மங்களின் பெயரிடல்
-
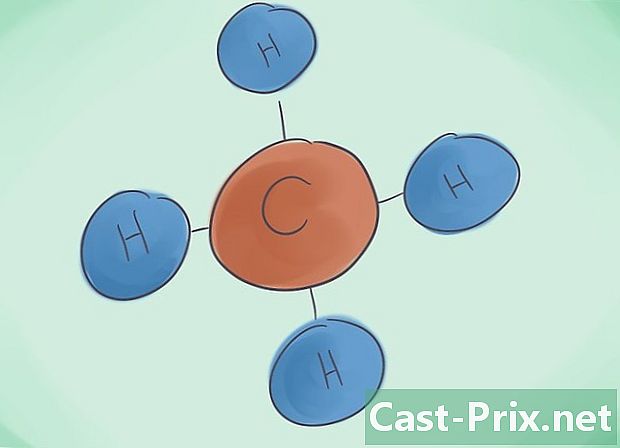
கோவலன்ட் கலவை என்றால் என்ன? கோவலன்ட் கலவைகள் குறைந்தது இரண்டு உலோகமற்ற கூறுகளின் இணைப்பால் விளைகின்றன. கலவையின் பெயர் அதை உருவாக்கும் எண் தரவுகளால் தீர்மானிக்கப்படுகிறது. இந்த பெயருக்கு அடுத்த கிரேக்க முன்னொட்டு சேர்மத்தில் உள்ள மூலக்கூறுகளின் எண்ணிக்கையைக் குறிக்கிறது. -
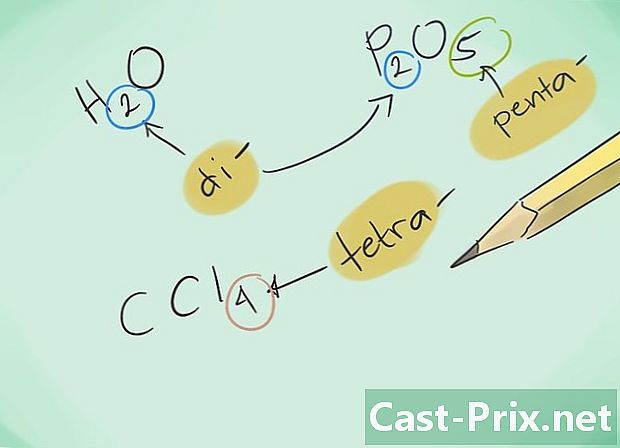
முன்னொட்டுகளுடன் உங்களைப் பழக்கப்படுத்துங்கள். 1 முதல் 8 அணுக்களின் சேர்மங்களுக்கான பின்வரும் முன்னொட்டுகளை நினைவில் கொள்ளுங்கள்:- 1 அணு - "மோனோ-"
- 2 அணுக்கள் - "டி-"
- 3 அணுக்கள் - "திரி-"
- 4 அணுக்கள் - "டெட்ரா-"
- 5 அணுக்கள் - "பென்டா-"
- 6 அணுக்கள் - "ஹெக்சா-"
- 7 அணுக்கள் - "ஹெப்டா-"
- 8 அணுக்கள் - "ஆக்டா-"
- பின்னர் சேர்மங்களுக்கு பெயரிடுங்கள். பொருத்தமான முன்னொட்டுகளைப் பயன்படுத்தி விளைந்த கலவைக்கு பெயரிடுக. பல அணுக்களைக் கொண்ட ஒரு சேர்மத்தை உருவாக்கும் ஒவ்வொரு உறுப்புகளிலும் முன்னொட்டுகள் ஒட்டப்பட வேண்டும்.
- எடுத்துக்காட்டு: CO கார்பன் மோனாக்ஸைட்டுக்குத் திரும்பும்2 கார்பன் டை ஆக்சைடை நியமிக்கும்.
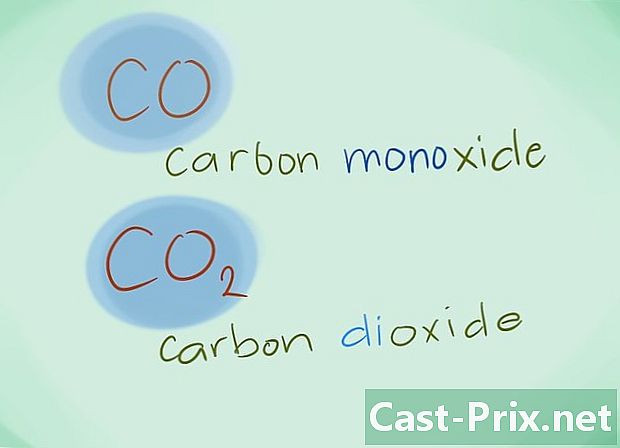
- எடுத்துக்காட்டு: என்2எஸ்3 நைட்ரஸ் ட்ரைசல்பைடுடன் ஒத்திருக்கும்.

- பெரும்பாலான சந்தர்ப்பங்களில், "மோனோ" என்ற முன்னொட்டை தவிர்க்கலாம்; இது, எந்த முன்னொட்டு இல்லாததை விடவும், பிந்தையது பயன்படுத்தப்பட வேண்டும் என்று தூண்டுகிறது. கார்பன் மோனாக்சைடு விஷயத்தில் இந்த முன்னொட்டு தொடர்ந்து பயன்படுத்தப்படுகிறது, இந்த பயன்பாடு வேதியியலின் முதல் ஒளிரும் நபர்களுக்கு செல்கிறது.
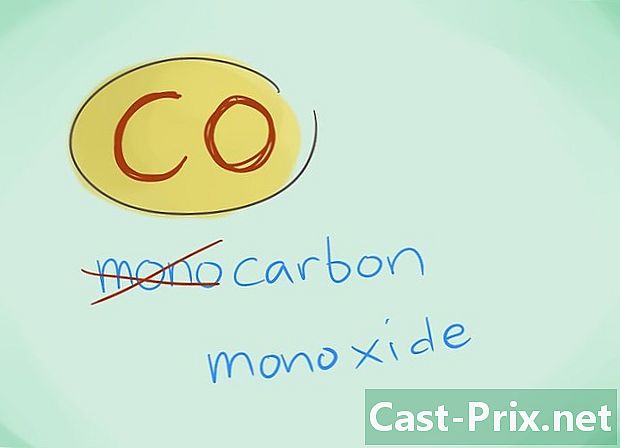
- எடுத்துக்காட்டு: CO கார்பன் மோனாக்ஸைட்டுக்குத் திரும்பும்2 கார்பன் டை ஆக்சைடை நியமிக்கும்.
- நிச்சயமாக, இந்த விதிகள் அனைத்திற்கும் பல விதிவிலக்குகள் பொருந்தும் என்று நீங்கள் சந்தேகிக்கிறீர்கள்; எடுத்துக்காட்டாக, இந்த சூத்திரம், CaCl2இது "கால்சியம் டைக்ளோரைடு" என்று அழைக்கப்படுகிறது, இது இல்லை. உங்கள் கலவை வெறுமனே கால்சியம் குளோரைடு என்ற பெயரை வைத்திருக்கும்.
- இவை அனைத்தும் கரிம வேதியியலுக்கு பொருந்தாது என்பதையும் கவனத்தில் கொள்ள வேண்டும்.
- இங்கே விரிவான விதிகள் வேதியியல் மற்றும் அறிவியலில் ஒரு தொடக்க பார்வையாளர்களை நோக்கமாகக் கொண்டுள்ளன. மாறி வேலன்ஸ் குறித்த விதிகளைப் போல மேம்பட்ட வேதியியல் நிலை வழியாக நீங்கள் செல்லும்போது மிகவும் மாறுபட்ட விதிகள் உள்ளன.